
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
Gilteritinib Fumarate
2023-12-02
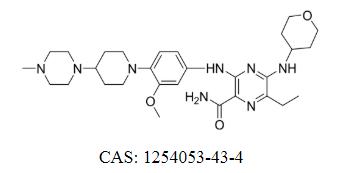
Gilteritinib Fumarate Cas: 1254053-43-4
1. Ιστορικό
Τα στοχευμένα φάρμακα για το Gillette (Gilteritinib) για ασθενείς με οξεία μυελογενή λευχαιμία ζουν περισσότερο, καλύτερα πρόσφατα που δημοσιεύθηκαν στο New England journal of ιατρική μιας μεγάλης κλινικής δοκιμής, τα αποτελέσματα δείχνουν ότι: σε σύγκριση με τη χημειοθεραπεία, η χρήση στοχευμένων φαρμάκων για το Gillette (Gilteritinib, όνομα εμπορεύματος Xospata), μπορεί να βελτιώσει το ποσοστό επιβίωσης των ασθενών με οξεία μυελογενή λευχαιμία (AML).
Τα αποτελέσματα της νέας δοκιμής είναι ενθαρρυντικά. Οι 371 ασθενείς που εγγράφηκαν στη δοκιμή ήταν ασθενείς με AML με ειδική μετάλλαξη του γονιδίου FLT3 που είχαν προηγουμένως υποβληθεί σε θεραπεία αλλά αργότερα υποτροπίασαν ή δεν ανταποκρίθηκαν στη θεραπεία (υποτροπιάζουσες/ανθεκτικές). Κατανεμήθηκαν τυχαία είτε σε θεραπεία με Gilteritinib είτε σε τυπική χημειοθεραπεία.
Τα αποτελέσματα έδειξαν ότι οι ασθενείς που έλαβαν θεραπεία για αποδοχή gillett, Gilteritinib όχι μόνο ζουν περισσότερο από ό,τι σε ασθενείς που υποβάλλονται σε χημειοθεραπεία (ο διάμεσος συνολικός χρόνος επιβίωσης ήταν 9,3 μήνες έως 5,6 μήνες) και είναι πιο πιθανό να επιτύχουν πλήρη ύφεση, ο αριθμός των λευκών αιμοσφαιρίων επανήλθε στο φυσιολογικό επίπεδο εν όλω ή εν μέρει (ασθενείς που έλαβαν Gilteritinib (34%), 15%) σε ασθενείς που υποβάλλονται σε χημειοθεραπεία.
2. Παρουσίαση
Το Gilteritinib Fumarate, που αναπτύχθηκε από την Astellas, εγκρίθηκε από τον Ιαπωνικό Οργανισμό Φαρμακευτικών Ιατρικών Συσκευών και Συσκευών (PMDA) στις 21 Σεπτεμβρίου 2018, στη συνέχεια εγκρίθηκε από τον Οργανισμό Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) στις 28 Νοεμβρίου 2018 και από τον Ευρωπαϊκό Οργανισμό Φαρμάκων (EMA) στις 24 Οκτωβρίου 2019 με την εμπορική ονομασία Xospata®. Το Gilteritinib έχει λάβει το καθεστώς ταχείας κυκλοφορίας και ορφανού φαρμάκου από τον FDA.
Το Gilteritinib Fumarate είναι ένας αναστολέας FLT3/AXL και το Xospata® είναι εγκεκριμένο για τη θεραπεία της υποτροπιάζουσας ή ανθεκτικής οξείας μυελογενούς λευχαιμίας με θετική μετάλλαξη FLT3.
Το Xospata® είναι ένα από του στόματος δισκίο που περιέχει 40 mg Gilteritinib. Η συνιστώμενη δόση είναι 120 mg μία φορά την ημέρα. Αυξήστε ή μειώστε τη δόση ανάλογα με την κατάσταση του ασθενούς, αλλά δεν πρέπει να υπερβαίνει τα 200 mg την ημέρα.
3. Σημείο στόχου
AXL; FLT3
4. Μηχανισμός δράσης
Αναστολείς υποδοχέα AXL. Αναστολείς FLT3
5. Ενδείξεις
Οξεία μυελογενής λευχαιμία
6. Στάδιο ανάπτυξης
Εγκρίθηκε για μάρκετινγκ στις 21 Σεπτεμβρίου 2018
7. Εταιρεία Ε&Α
Αστέλλας
8. Διαδρομή Σύνθεσης
8.1. Η αρχική διαδρομή
8.2. Η διαδρομή μας (βελτιστοποιημένη) - Καλύτερη σταθερότητα και υψηλότερη απόδοση
8.3. Ros of KSM [CAS 2043020-03-5]
8.4. Σύντομη διαδικασία παραγωγής [CAS 2043020-03-5]
Βήμα 1:
Σε ένα εναιώρημα NaOH προστέθηκε 3-οξοπεντανοϊκός αιθυλεστέρας σε μία δόση, και στη συνέχεια το μίγμα της αντίδρασης αναδεύτηκε σε θ.δ. Προστέθηκε διάλυμα NaNO2 σε νερό και στη συνέχεια προστέθηκε στάγδην H2SO4. Ένα διάλυμα NaOH προστέθηκε στάγδην και το προκύπτον μίγμα εκχυλίστηκε με ΜΤΒΕ. Οι συνδυασμένες οργανικές στιβάδες πλύθηκαν με άλμη, ξηράνθηκαν υπεράνω Na2S04, διηθήθηκαν και συμπυκνώθηκαν για να δώσουν το προϊόν (Ε)-2-οξοβουτανική οξίμη.
Βήμα 2:
Ένα εναιώρημα (Ε)-2-οξοβουταναλικής οξίμης και αμινομαλονονιτριλίου ρ-τολουολοσουλφονικού οξέος σε ΙΡΑ) αναδεύτηκε σε θ.δ. υπό αργό. Αφού ελέγχθηκε με TLC, το μίγμα της αντίδρασης διηθήθηκε, το κέικ πλύθηκε με ΙΡΑ και νερό, και ξηράνθηκε για να δώσει 1-οξείδιο 2-αμινο-3-κυανο-5-αιθυλοπυραζίνης.
Βήμα 3:
Σε ένα εναιώρημα 1-οξειδίου 2-αμινο-3-κυανο-5-αιθυλοπυραζίνης σε άνυδρο DMF προστέθηκε POCl3 στους 0oC. Το προκύπτον μίγμα αναδεύτηκε στους 80oC. Αφού ελέγχθηκε με TLC το μίγμα της αντίδρασης προστέθηκε σε πάγο/νερό αργά και εκχυλίστηκε με ΜΤΒΕ. Οι συνδυασμένες οργανικές στιβάδες πλύθηκαν με άλμη, ξηράνθηκαν υπεράνω Na2S04, διηθήθηκαν και συμπυκνώθηκαν για να δώσουν 3-αμινο-5-χλωρο-6-αιθυλοπυραζινο-2-καρβονιτρίλιο.
Βήμα 4:
Σε ένα εναιώρημα t-BuONO και CuBr2 σε DMF προστέθηκε ένα διάλυμα 3-αμινο-5-χλωρο-6-αιθυλοπυραζινο-2-καρβονιτριλίου σε DMF στάγδην. Αφού ελέγχθηκε με TLC το μίγμα της αντίδρασης ψύχθηκε σε θ.δ., και στη συνέχεια χύθηκε σε πάγο/νερό, εκχυλίστηκε με ΜΤΒΕ. Οι συνδυασμένες οργανικές στιβάδες πλύθηκαν με άλμη, ξηράνθηκαν πάνω από Na2S04, διηθήθηκαν και συμπυκνώθηκαν για να δώσουν ακατέργαστο προϊόν το οποίο καθαρίστηκε με χρωματογραφία για να δώσει 3-βρωμο-5-χλωρο-6-αιθυλοπυραζινο-2-καρβονιτρίλιο.
9. Κατάλογος ενδιάμεσων προϊόντων που μπορούμε να προμηθεύσουμε
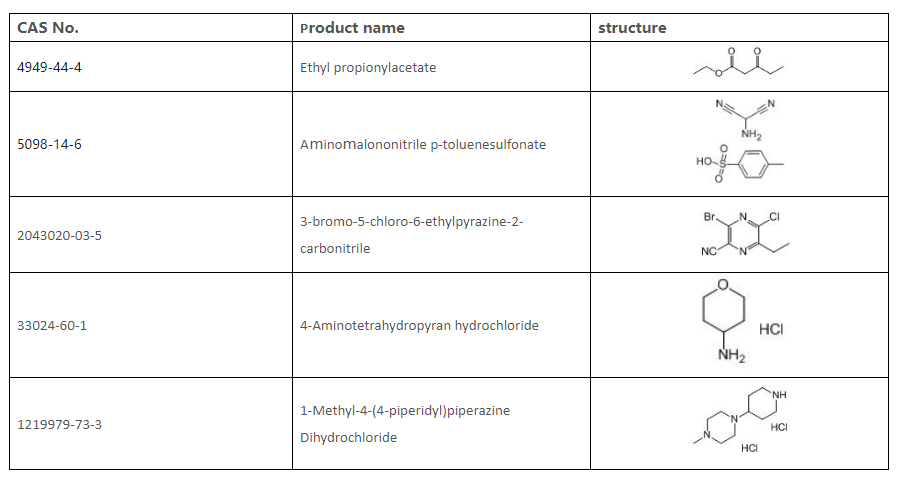
Η Sandoo Pharmaceutica είναι επαγγελματίας κατασκευαστής φαρμακευτικών ενδιάμεσων προϊόντων. Παρέχουμε καλής ποιότητας Gilteritinib Fumarate Cas: 1254053-43-4. Καλώς ήρθατε και περιμένουμε την ερώτησή σας!




